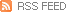안녕하세요
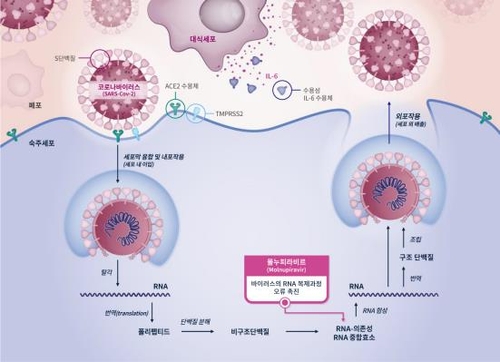
한미약품과 셀트리온, 동방에프티엘 이상 국내 기업 세 곳이 머크앤드컴퍼니(MSD)가 개발한 코로나19 먹는 치료제 몰누피라비르(제품명 라게브리오)의 복제약(제네릭 의약품) 생산을 할 수 있게 됐습니다.
보건복지부는 이들 3개 기업이 라게브리오 복제약을 생산해 105개 중저소득 국가에 공급한다고 20일 발표했는데 한미약품은 원료와 완제품을 모두 생산하며, 셀트리온은 완제품을, 동방에프티엘은 원료를 생산하고 이들이 생산하는 약은 국내 공급용은 아닌 것으로 알려졌습니다.
한미약품 원료의약품 계열사 한미정밀화학은 라게브리오 생산에 즉각 착수했는데 생산된 원료는 경기도 팔탄 소재 한미약품 스마트플랜트로 옮겨져 완제의약품 생산에 투입됩니다.
셀트리온의 라게브리오 완제품 개발과 생산은 계열사인 셀트리온제약이 맡고, 해외 공급을 셀트리온이 담당하는데 셀트리온제약은 연내 제품 개발을 완료한다는 목표로 이미 제형 연구에 착수했습니다.
생동성 시험과 허가 등 상업화를 위한 절차를 거쳐 충북 청주공장에서 제품을 생산할 예정인데 셀트리온은 이번 기술 도입으로 중저소득국에 라게브리오 제네릭을 공급하고 유럽 등 선진국에는 항체치료제 '렉키로나'를 판매한다는 전략으로 선진국과 중저소득국 전부를 시장으로 가져가겠다는 전략입니다
정부는 "국내 기업의 우수한 의약품 품질관리 및 생산역량 등을 국제적으로 인정받은 결과"라고 설명했습니다.
국제의약품특허풀(MPP)이 코로나19 먹는 치료제 생산기업으로 선정한 곳은 한국 중국 인도 등 전 세계 총 11개국 27개 기업으로 MPP는 각 기업이 복제약을 제조해 저렴한 가격으로 공급할 수 있도록 의약품 특허권 소유자와 라이선스 계약을 체결하는 국제협력단체로 화이자 먹는 치료제에 대해서는 현재 심사가 진행 중이며 추후 생산 기업 선정 결과를 발표할 예정이지만 화이자가 응할지는 미지수입니다.
권덕철 보건복지부 장관은 "코로나19 백신과 함께 먹는 치료제의 생산·공급을 통해 전 세계 코로나19 종식에 한국 기업이 기여하게 된 것을 기쁘게 생각한다"며 "국내 생산을 위한 지원을 아끼지 않겠다"고 밝혔습니다.
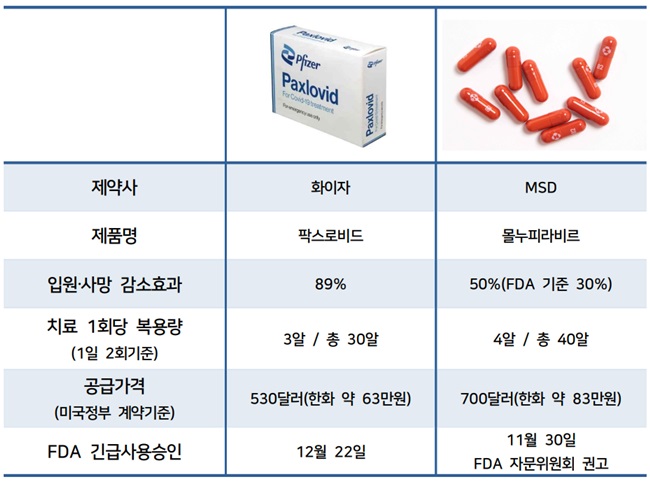
다만 머크사(MSD)의 경구용 코로나19치료제 라게브리오의 효과가 화이자 먹는 치료제"팍스로비드"에 비해 현저하게 떨어지는 것으로 알려져 있고 적용에 제약조건이 많은 것으로 알려져 있어 얼마나 효과가 있을 지는 의문인 상황입니다
국내 재약사와 바이오신약 개발사들도 올 해 안으로 신규 치료제와 백신 국산화를 달성할 것으로 예상되고 있어 우리나라가 코로나19 치료와 예방에 허브 국가가 될 것 같습니다
투자에 참고하세요



'주식시장이야기' 카테고리의 다른 글
| 한국산 무기수출 아랍에미리트는 되고 이집트는 안되는 이유 (0) | 2022.01.21 |
|---|---|
| 뉴스토마토 오는 25일 '2022 넥스트 비즈 컨퍼런스' 개최 (0) | 2022.01.21 |
| 오토앤 올 해 첫 공모주 상장 첫날 상한가 (0) | 2022.01.20 |
| 기산텔레콤 무인항공기 기술 보유 부각 장중 상한가 (0) | 2022.01.20 |
| 메타버스 관련주 정부 ‘메타버스 신산업 선도전략’ 발표 수혜 기대감 (0) | 2022.01.20 |