안녕하세요
윤석열 정부에서 비대면진료에 대한 입법이 구체화되면서 대형병원들의 숙원사업이 이뤄질 것으로 보입니다
코로나19팬데믹 와중에 감염병 특성 상 비대면진료의 필요성으로 한시적으로 허용되었지만 코로나19팬데믹이 끝나기 전에 관련 입법을 진행해 원격진료가 가능하게 만들겠다고 윤석열 정부와 국민의힘이 나서고 있습니다
원격진료라는 말에 거부감이 있어 비대면진료라는 단어를 사용하고 있는데 서울중앙병원과 삼성의료원, 세브란스 같은 대형병원들은 지방에 있는 환자를 비대면진료를 통해 의료서비스를 제공할 수 있어 수익 확대의 길이 열리게 될 것 같습니다
애초 비대면진료서비스는 의료사각지대인 지방오지와 도서벽지, 이동이 불편한 장애인들이 대상이었지만 지금 국회에서 논의하는 것은 대형병원의 이익을 대변하는 규제없는 비대면진료로 지방병의원과 서울의 중소형 병원들은 그 만큼 환자를 대형병원에 빼앗길 수 밖에 없는 상황이 도래할 수 있습니다
기본적으로 비대면진료는 민간의료보험의 가입을 전제로 하고 있어 삼성생명과 삼성화재 같은 보험사들의 실적에도 긍정적일 수 있는데 그렇기 때문에 국내 재벌들은 비대면의료서비스의 허용을 줄기차게 요청해 왔습니다
30년 넘게 규제로 막혀 있던 비대면 진료(원격의료)가 합법화되면서 유비케어가 비대면의료시장의 수혜를 입을 것으로 예상되기 때문에 매수세가 유입되고 있습니다
보건복지부는 이날부터 대한의사협회와 의료현안협의체를 구성해 매주 지역 및 필수의료 강화, 의학교육 및 전공의 수련체계 발전방안 등 의료계 현안을 논의한다고 예고했는데 코로나19로 한시 허용됐던 비대면 진료를 제도화하는 방안도 논의될 것으로 알려졌습니다.
코로나19로 한시 허용된 사이 닥터나우, 닥터콜, 솔닥 등 비대면 진료를 중개하는 플랫폼이 대거 늘어나고 국민 여론이 긍정적으로 바뀌자 정부는 의료법 개정을 통한 비대면 진료 제도화에 드라이브를 걸고 있는데 윤석열 정부가 출범 이후 110대 국정과제에 '비대면 진료 제도화'를 포함했고, 실내마스크 착용 의무 해제 등 엔데믹 전환 국면에 접어들며 연내 제도화 기대감도 제기되고 있습니다
윤석열 정부에서 디지털헬스케어 시장 활성화를 정책 주요 과제로 제시하고 있지만 그 이면에는 디지털헬스케어에 막대한 자본을 투자할 수 있는 재벌계열 대형병원과 기존 시장을 선점하고 있는 대형대학병원들의 이익이 숨겨져 있고 궁극적으로 영리병원 허용과 민간보험 활성화 장기적으로 전국민의료보험 무력화를 향해 가고 있는 것입니다
우리나라도 전국민의료보험이 무력화될 경우 미국처럼 돈이 없으면 적당한 의료서비스를 받지 못하는 나라가 될 가능성이 커 민간보험을 가입해 두는 것이 의료서비스를 받는데 도움이 될 것입니다
유비케어는 간편 병·의원 예약접수 모바일 서비스 '똑닥'을 만든 비브로스 지분을 지난 2016년 11월에 취득하면서 대표적인 원격의료 관련주로 떠올랐고 이지케어텍(13.7%), 인피니트헬스케어(6.2%) 등 원격의료 관련주로 묶인 기업들도 동반 상승하고 있습니다.
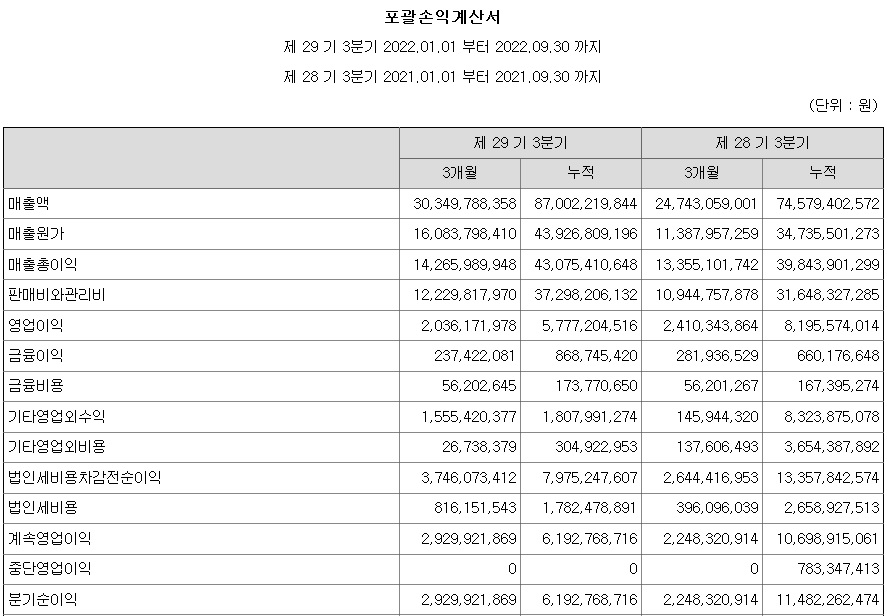
유비케어의 지난 해 3분기 실적기준 적정주가는 9,000원으로 평가되어 실적호전과 비대면진료 입법을 재료로 주가재평가가 이뤄지고 있는 모습입니다
투자에 참고하세요



'주식시장이야기' 카테고리의 다른 글
| 유니크 중동국가 수소경제 투자 급증 수혜 기대감 (0) | 2023.01.31 |
|---|---|
| SBS콘텐츠허브 월트디즈니와 10년간 SBSTV드라마 1편 공급계약 체결 급등세 (0) | 2023.01.31 |
| 미국 포드 전기차 가격인하 단행 테슬라가 벌인 전기차 가격인하 전쟁 동참 현대차와 기아 미국 전기차 시장 퇴출 가능성 (0) | 2023.01.31 |
| 미국증시 미연준 피봇 준비 안되어 있다는 의견에 동반 급락세 (0) | 2023.01.31 |
| 윤석열 정부 한국산업은행 법 개정 전 부산이전 강행 추진 한국산업은행법 무시 뭐가 그리 급한가? (0) | 2023.01.30 |