링크를 타고 유튜브에서 시청 부탁드립니다. 좋아요 구독은 더 좋은 콘텐츠 제작에 큰 힘이 됩니다
안녕하세요
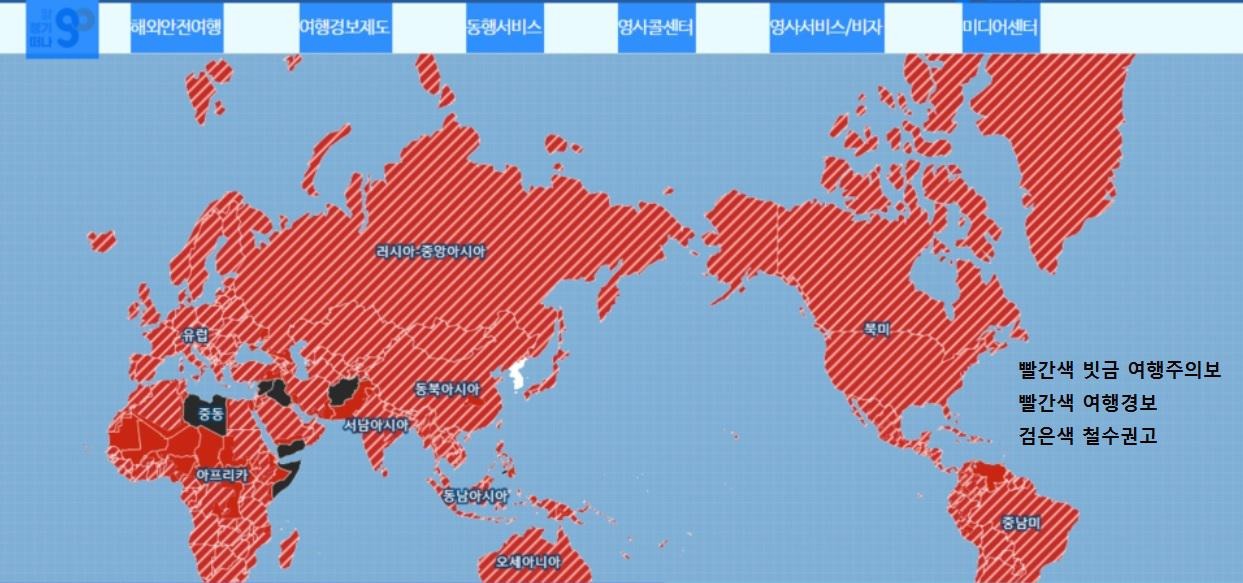
네오이뮤텍은 12일 NT-I7의 위암(임상 2상), 고위험 피부암(임상 1b/2a상), 교모세포종(임상 1상) 등의 적응증에 대해 임상을 중단한다고 갑자기 공시했습니다.
위암 임상 2상은 68명을 대상으로 지난 2021년 1월 21일에 시작해 오는 10월 17일까지 진행될 예정이었는데 해당 임상은 미국 식품의약국(FDA), 유럽의약품청(EMA) 임상 2상입니다.
네오이뮨텍 측은 “임상 개시 당시와 비교해 위암 적응증 치료 환경이 변화해 기존 대조군 비교 임상 진행이 불가하다”면서 “면역관문 억제제에서는 효과를 입증하지 못한 다른 적응증에 선택과 집중을 하기 위해 다국가 임상으로 확장 시험을 본격 진행하기 전, 해당 임상을 중도 중단하는 것으로 의사 결정했다”고 밝혔습니다.
무슨 뜻인지 모르게 어렵게 꼬아 놓았는데 위암 치료제로 효능과 효과를 확인하기 어렵고 투자비만 날리는 임상이 될 수 있어 조기 중단하는 것으로 결국 실패했다는 의미로 받아들여집니다
흑색종·메르켈 세포암 (MCC)·피부 편평 세포암 (cSCC) 적응증으로 진행 중이던 NT-I7 FDA 임상 1b/2a상도 위암과 같은 이유로 임상을 중단했는데 고위험 피부암 임상은 지난 2019년말 시작해 올해 말까지 진행할 예정이었습니다.
교모세포종 FDA 임상 1상도 중단했는데 이 임상은 지난 2018년 2월에 시작했습니다.
앞에서도 설명했지만 바이오신약개발사들이 신약개발을 마라톤에 비유하며 오랜동안 시장을 통해 자금을 조달하고 연구개발로 탕진하는 방식은 더 이상 시장참여자들의 인내심이 허락하는 방식이 아닌 것으로 코로나19백신과 치료제 개발 과정에 신약개발이 그렇게 오랜 시간이 필요한 사업이 아니란 사실을 투자자들이 알아버렸기 때문에 "네오이뮨텍"의 신약개발고 같이 중간에 라이센스 아웃을 하지 않고 독자적으로 임상을 진행하는 경우는 연구의 진실성에서 의구심을 사기 때문에 이제는 더 이상 시장으로부터 자금을 조달받기 어려워 진 것입니다
바이오신약 개발에 있어 기존 개념이 구식이 되어 투자자들이 더 이상 인내심을 갖고 바이오신약 개발사들을 기다려주지 않는다는 사실을 깨달아야 합니다
시장에서 개발비를 조달하기 쉬웠다면 네오이뮨택은 결코 임상을 중당하지 않고 그대로 진행해 투자자들의 투자금을 낭비했을 겁니다
이제는 바이오신약개발사 투자에 있어 라이센스 아웃을 통해 연구진실성을 객관적으로 평가받고 신약의 가치를 중간 점검 받는 과정이 필수로 필요해 보입니다
아울러 네오이뮨텍의 임상 실패 가능성이 공시 이전에 사외로 유출된 정황이 엿보이는데 외국인투자자들이 공시 이전에 집중적으로매도하여 주가하락의 위험을 회피한 것으로 정보의 비대칭성 이슈를 제기하게 만들고 있습니다
외국인투자자들의 집중적인 매도로 52주 신저가 행진을 벌이고 있는데 주가하락은 저가매수의 기회로 작용하기도 하는데 일본정부의 후쿠시마원전 방사능 오염수 해양폐기가 윤석열의 공개적인 찬성으로 가시화되면서 네오이뮨텍이 개발하고 있는 ARS치료제가 모멘텀이 될 수 있다는 막연한 기대감을 갖게 합니다
투자자들은 이벤트가발생했을 때 관련주 찾기에 있어 그럴듯한 근거를 선호하는데 ARS치료제 개발은 나름 의미 있는 매수이슈가 될 수 있기 때문입니다
하지만 미국 국방성이 기존 미국 제약사의 ARS치료제가 있는데 굳이 비축용으로 네오이뮨텍의 ARS치료제를 구매할 지는 의문이 들고 있습니다
투자에 참고하세요












'주식시장이야기' 카테고리의 다른 글
| '주가조작 패가망신법' 국회 통과 윤석열 정부 주가조작 엄단 쇼하지 마라 (0) | 2023.07.14 |
|---|---|
| 미국증시 생산자물가지수PPI 하락 인플레이션 압력감소로 일제히 상승세 (0) | 2023.07.14 |
| 포스코 2030년 합산 매출 100조원 목표 제시 실적증가 기대감 (0) | 2023.07.13 |
| 엠플러스 2차전지 조립공정장비업체 주거래처 SK온 미국공장 발주 수혜 기대감 (0) | 2023.07.13 |
| 아이쓰리시스템 군사용 적외선영상 센서 독점 생산 방산시장 성장 수혜 (0) | 2023.07.13 |